
神经科学研究的核心挑战在于,如何能在某一时刻只控制某一类神经元的活动。光遗传学技术应凭借高时空分辨率的独特优势,已成为解析神经环路功能的关键手段。
光遗传双向调控元件通过将两种光谱分离度高的激活型与抑制型光敏蛋白的编码序列整合在同一表达载体中,再通过病毒载体递送至目标神经元。利用不同波长光线的特异性激发,分别触发神经元的激活或抑制效应,双向调控神经元的电活动状态。光电流强度大、激活 / 抑制光谱无交叉干扰、适配病毒载体的有效载荷。从早期单一功能光敏蛋白到新一代双向调控元件的技术迭代,解决了传统光遗传工具无法同时实现双向操控的痛点,极大拓展了实验设计的灵活性。它兼具细胞特异性强、响应速度快、调控可逆的特点,能够在活体动物上实现对特定神经环路功能的精准解析,是神经科学基础研究与转化应用的重要利器。目前,eNPAC2.0和somBiPOLES是科研领域广泛应用的两类主流光遗传双向调控元件。
橙/红光(590-620 nm)照射时,NpHR作为离子泵发挥抑制效应,通过转运离子抑制神经元动作电位的产生。蓝光(448 nm)照射时,ChR2被激活,阳离子内流触发神经元快速放电。胆碱能神经元功能研究在ChAT-Cre小鼠的内侧隔核(MS)中表达eNPAC2.0,可通过光脉冲响应区分ChAT+与ChAT-细胞,解析胆碱能神经元的放电规律。
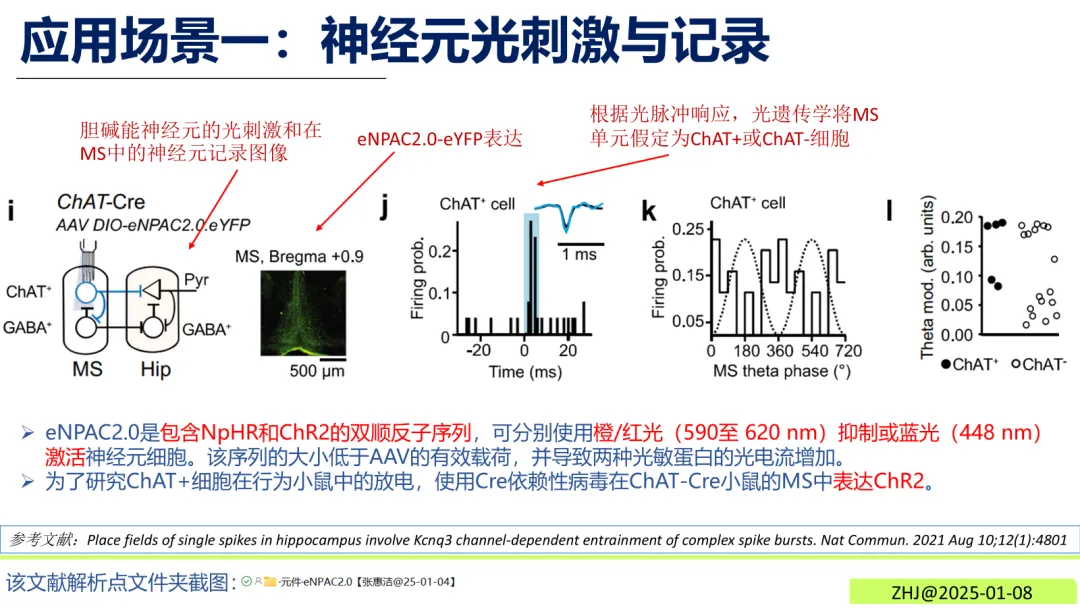 图1 神经元光刺激与记录
图1 神经元光刺激与记录
将eNPAC2.0双侧注射至Rpb4-cre小鼠的后内侧皮层(RSP),以2 Hz节律交替施加蓝光与黄光刺激,可模拟氯胺酮诱导的神经元活动模式,减弱感觉与情感反应的关联。
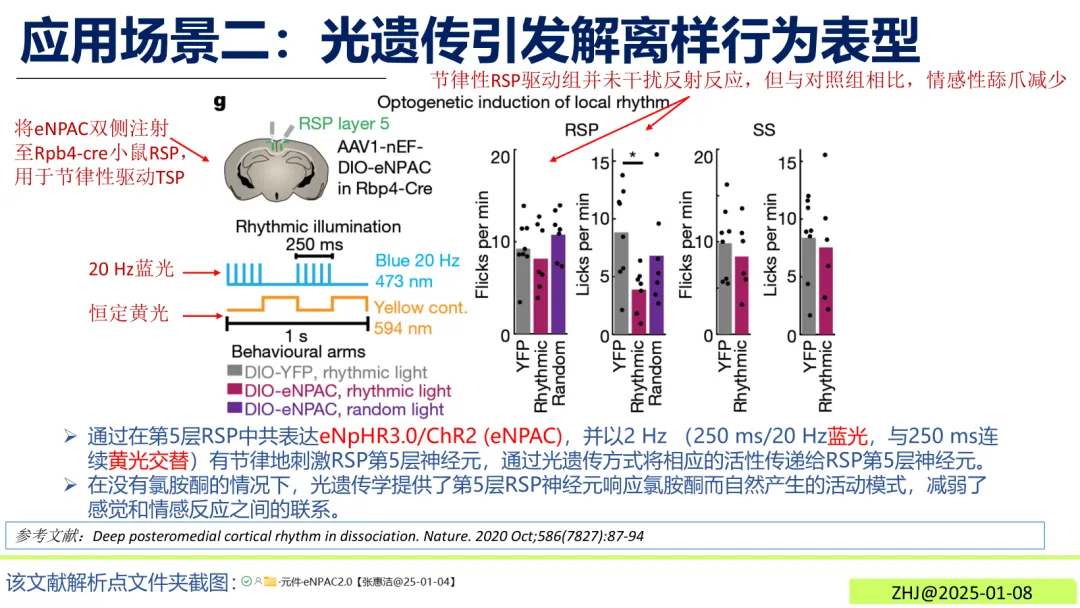
图2 光遗传引发解离样行为表型
觅食行为环路解析在Sst-Cre小鼠中,通过黄光(593 nm)抑制表达eNPAC2.0的LSssT-LH投射神经元,可观察到小鼠进入食物区的潜伏期增加、次数减少,直接验证该通路对觅食行为的必要性。图3觅食行为必要途径
somBiPOLES是由蓝光激活的抑制型光敏蛋白“GtACR2”与红光激活的激活型光敏蛋白“Chrimson”融合而成的新型元件。相比原型BiPOLES,它通过连接羧基末端的“kv2.1转运序列”实现体细胞靶向表达,仅分布于细胞体与近端树突,避免了核内定位问题,同时提升了光电流强度。其核心优势在于抑制性阴离子与兴奋性阳离子电流的峰值具有最大光谱分离度,操控精准度更高。
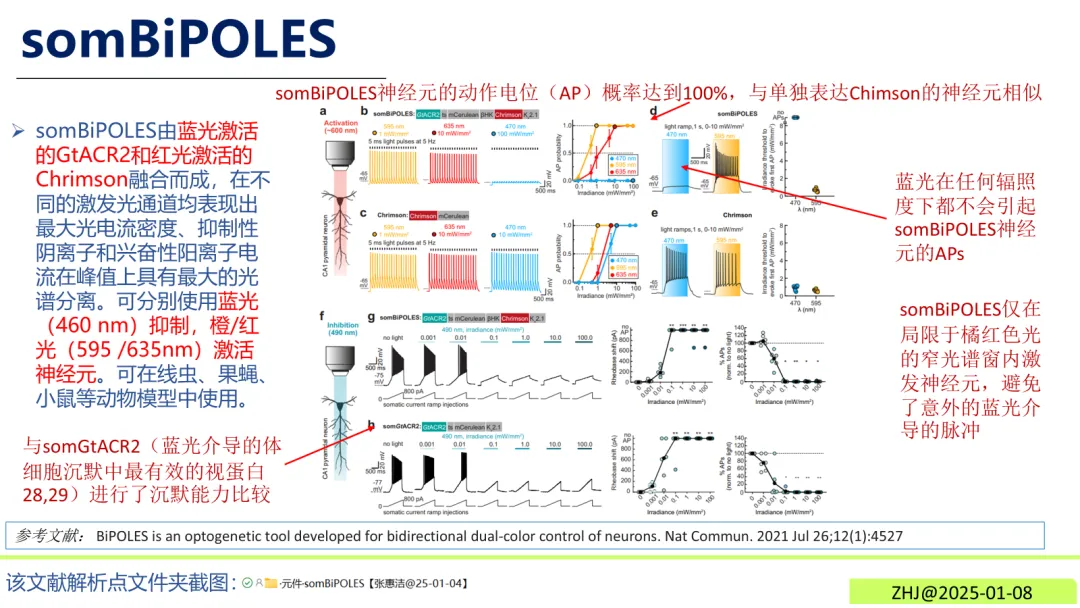
图4 somBiPOLES
蓝光(460 nm)照射激活GtACR2,阴离子内流快速沉默神经元,抑制神经元活动。橙/红光(595/635 nm)照射激活Chrimson,阳离子内流高效诱发神经元动作电位。
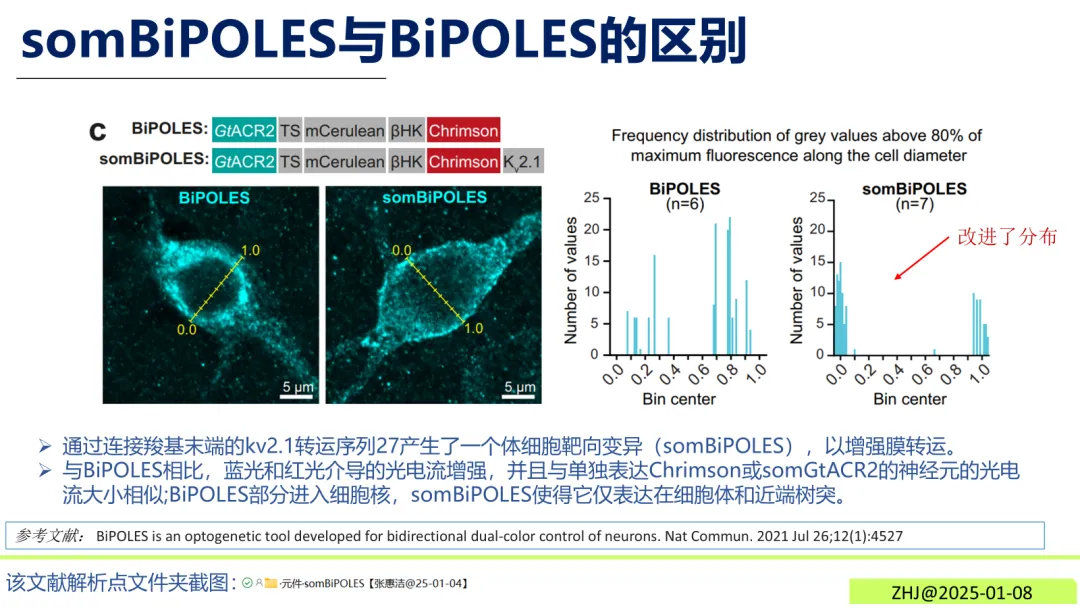
图5 somBiPOLES与BiPOLES的区别
小鼠海马体CA1区,将somBiPOLES表达于VIP中间神经元,同时在锥体神经元中表达CheRiff。红光可特异性激活VIP神经元,蓝光则精准激活锥体神经元,实现同一视野内两种神经元群的无交叉调控。
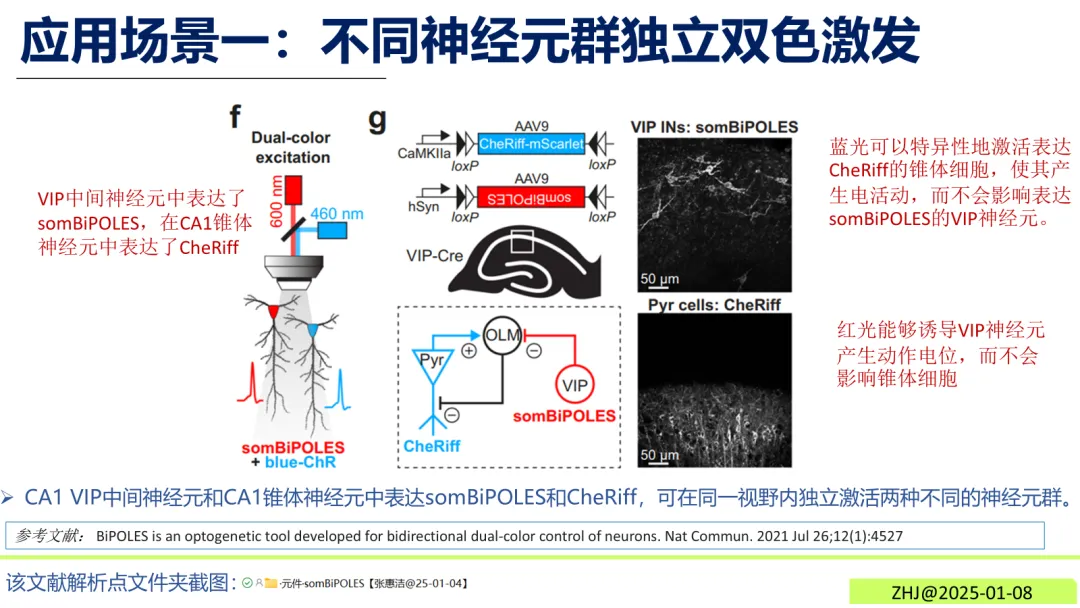
图6 不同神经元群独立双色激发
无脊椎动物的运动调控研究发现,在线虫模型中,红光照射可引发体壁肌肉收缩,蓝光则触发身体伸展,清晰解析胆碱能运动神经元的激活与抑制效应。
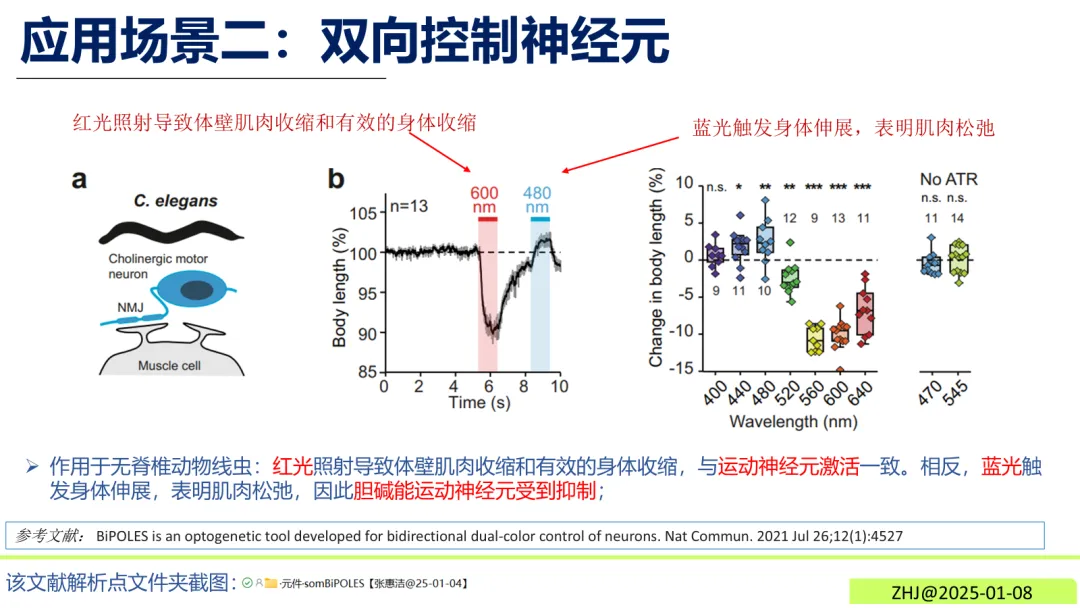
图7 双向控制神经元
TH-Cre小鼠的蓝斑核(LC)神经元中表达somBiPOLES,橙色光(594 nm)照射可触发瞳孔扩张,标志着觉醒状态激活;施加蓝光(473 nm)则可立即逆转该效应,实现对觉醒通路的动态双向操控。
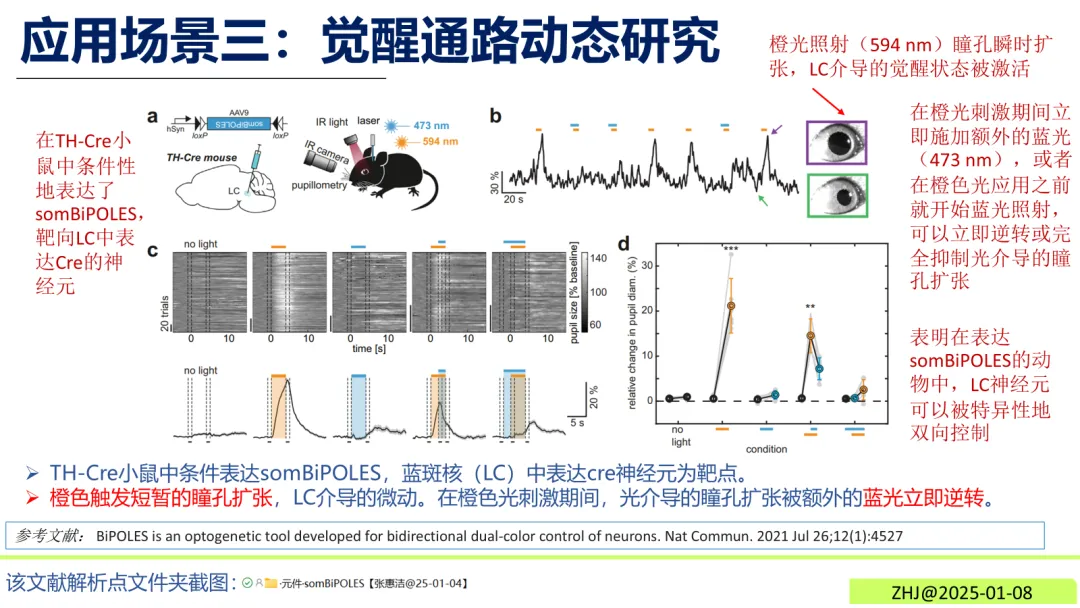
图8 觉醒通路动态研究
光遗传双向调控元件作为神经元操控工具可精准作用于特定脑区的靶细胞,响应时间以毫秒级计算,远超传统药理学手段;同一元件可通过切换光照波长实现神经元的激活与抑制,且效应具有可逆性;从线虫、果蝇等无脊椎动物,到小鼠等哺乳动物,均可稳定发挥调控作用,适用范围广泛。从eNPAC2.0到somBiPOLES,光遗传双向调控元件的持续优化,随着元件设计的不断升级,其在脑疾病模型构建、神经调控治疗等领域的转化应用价值将愈发凸显。